Bateria alcalina recargable Cobre Hierro.
- Sergi
- Mensajes: 1723
- Registrado: Vie Mar 17, 2006 10:35 am
- País: El Segrià
- Ciudad: Lleida
- Ubicación: (a la derecha, según se mira, de la Vía Láctea)
- Contactar:
Re: Bateria alcalina recargable Cobre Hierro.
uups... la he liado con la corrección ortográfica y he duplicado el mensaje. Tal vez un poco más de tiempo para corregir errores estaría bien.
"La manzana no nos echó del paraiso, sólo nos dejó ciegos para verlo"
Cecil Thousan
Cecil Thousan
- Sergi
- Mensajes: 1723
- Registrado: Vie Mar 17, 2006 10:35 am
- País: El Segrià
- Ciudad: Lleida
- Ubicación: (a la derecha, según se mira, de la Vía Láctea)
- Contactar:
Re: Bateria alcalina recargable Cobre Hierro.
Hola a tod@s
Sigo peleando con los electrolitos y los electrodos.
Después de decenas de pruebas he llegado a algunas conclusiones sobre la batería de flujo de hierro.
Utilizar cloruro de hierro III comercial al 40% en las dos semiceldas no funciona. Después de días de ciclado (carga y descarga) con electrodos de grafito esponjoso, tanto en el positivo como en el negativo, no produjo ninguna carga significativa ni rendimiento. Cargando hasta los 3,5v, 11.000 mAh y descargando a razón de 300mA caía rápidamente la tensión y sumaba apenas 4 mAh.
La tensión de trabajo con grafito y FeCl3 en las dos semiceldas, después de más de un día de carga, y después de unas pocas horas de reposos, es de unos 0,1v. Y sin apenas capacidad de descarga.
La conclusión que saco es que no se puede balancear el electrolito, pues no tiene donde desplazar los -Cl. La explicación que doy a la capacidad de balancear el electrolito y formar FeCl2 (verde) en las pruebas de Schopen es que se disolvía parte del electrodo negativo, pero al utilizar poco electrolito, apenas unas decenas de cm3, no disolvía completamente el electrodo de hierro.
Pero no se puede trabajar con grandes cantidades de electrolito (flujo) sin disolver completamente los electrodos negativos.
La semicelda positiva trabaja bien con cloruro de hierro III y electrodo de grafito esponjoso. Falta solucionar la semicelda negativa. Pero usar un electrolito a base de otra sustancia es un problema de difusión y mezclas de electrolitos a la larga.
Sigo peleando con los electrolitos y los electrodos.
Después de decenas de pruebas he llegado a algunas conclusiones sobre la batería de flujo de hierro.
Utilizar cloruro de hierro III comercial al 40% en las dos semiceldas no funciona. Después de días de ciclado (carga y descarga) con electrodos de grafito esponjoso, tanto en el positivo como en el negativo, no produjo ninguna carga significativa ni rendimiento. Cargando hasta los 3,5v, 11.000 mAh y descargando a razón de 300mA caía rápidamente la tensión y sumaba apenas 4 mAh.
La tensión de trabajo con grafito y FeCl3 en las dos semiceldas, después de más de un día de carga, y después de unas pocas horas de reposos, es de unos 0,1v. Y sin apenas capacidad de descarga.
La conclusión que saco es que no se puede balancear el electrolito, pues no tiene donde desplazar los -Cl. La explicación que doy a la capacidad de balancear el electrolito y formar FeCl2 (verde) en las pruebas de Schopen es que se disolvía parte del electrodo negativo, pero al utilizar poco electrolito, apenas unas decenas de cm3, no disolvía completamente el electrodo de hierro.
Pero no se puede trabajar con grandes cantidades de electrolito (flujo) sin disolver completamente los electrodos negativos.
La semicelda positiva trabaja bien con cloruro de hierro III y electrodo de grafito esponjoso. Falta solucionar la semicelda negativa. Pero usar un electrolito a base de otra sustancia es un problema de difusión y mezclas de electrolitos a la larga.
"La manzana no nos echó del paraiso, sólo nos dejó ciegos para verlo"
Cecil Thousan
Cecil Thousan
Re: Bateria alcalina recargable Cobre Hierro.
Pues vaya.
Esa era la prueba que planeaba:
Hacer de grafito ambos electrodos y poner Fe3Cl en un vaso y HCl en el otro .
Entonces si al descargar pasan Cl- al otro lado cambiando el hierro de oxidación 3 a 2 y cerrando el circuito por los electrodos.
Esto no tendría deposiciones ni cambios en los electrodos, pero imagino que el voltaje será muy bajo.
Esa era la prueba que planeaba:
Hacer de grafito ambos electrodos y poner Fe3Cl en un vaso y HCl en el otro .
Entonces si al descargar pasan Cl- al otro lado cambiando el hierro de oxidación 3 a 2 y cerrando el circuito por los electrodos.
Esto no tendría deposiciones ni cambios en los electrodos, pero imagino que el voltaje será muy bajo.
- Sergi
- Mensajes: 1723
- Registrado: Vie Mar 17, 2006 10:35 am
- País: El Segrià
- Ciudad: Lleida
- Ubicación: (a la derecha, según se mira, de la Vía Láctea)
- Contactar:
Re: Bateria alcalina recargable Cobre Hierro.
Buenas alberttoy
Con HCl puro (entiendo que al 24% "salfuman") en la semicelda negativa no lo he probado. Puede ser un dato interesante.
Los ciclos de carga y descarga son tremendamente largos. La última prueba ha estado descargando más de 30 horas seguidas a 300mA. unos 8.000 mAh. Estoy probando con electrolido con zinc y sin zinc. Con NaCl y sin sal... ya os pasaré resultados cuando tenga datos concluyentes.

Mientras tanto, sigo con los preparativos del nuevo prototipo de batería de flujo. Este si con capacidad de bombeo de electrolito y espero que más intensidad de carga y descarga. De momento he probado la hermeticidad de todo el conjunto lleno de agua y sometiéndolo a presión de 1 atm. Todo correcto.
Estoy esperando que me lleguen las nuevas bombas peristàlticas para conectar los dos circuitos por separado.
Con HCl puro (entiendo que al 24% "salfuman") en la semicelda negativa no lo he probado. Puede ser un dato interesante.
Los ciclos de carga y descarga son tremendamente largos. La última prueba ha estado descargando más de 30 horas seguidas a 300mA. unos 8.000 mAh. Estoy probando con electrolido con zinc y sin zinc. Con NaCl y sin sal... ya os pasaré resultados cuando tenga datos concluyentes.

Mientras tanto, sigo con los preparativos del nuevo prototipo de batería de flujo. Este si con capacidad de bombeo de electrolito y espero que más intensidad de carga y descarga. De momento he probado la hermeticidad de todo el conjunto lleno de agua y sometiéndolo a presión de 1 atm. Todo correcto.
Estoy esperando que me lleguen las nuevas bombas peristàlticas para conectar los dos circuitos por separado.
"La manzana no nos echó del paraiso, sólo nos dejó ciegos para verlo"
Cecil Thousan
Cecil Thousan
Re: Bateria alcalina recargable Cobre Hierro.
Hay unas bombas de recirculación, que llevan una bola de plástico, evidentemente con núcleo ferromagnético como única pieza móvil; no deben ser muy caras, se usan en fontanería, quizás te puedan servir mejor que las peristálticas.
Sigo el tema con interés por si me sirve de algo, pero tal como están las cosas por ahí, pienso que lo mejor en plan aficionado es pensar en metal-aire, y en concreto hierro-aire.
Saludos.
Sigo el tema con interés por si me sirve de algo, pero tal como están las cosas por ahí, pienso que lo mejor en plan aficionado es pensar en metal-aire, y en concreto hierro-aire.
Saludos.
Cielo azul sobre campo de mieses, ánimo.
Constitución Española:
Todos los españoles tienen el deber de trabajar y el derecho al trabajo.
Todos los españoles tienen derecho a disfrutar de una vivienda digna y adecuada.
Constitución Española:
Todos los españoles tienen el deber de trabajar y el derecho al trabajo.
Todos los españoles tienen derecho a disfrutar de una vivienda digna y adecuada.
- Sergi
- Mensajes: 1723
- Registrado: Vie Mar 17, 2006 10:35 am
- País: El Segrià
- Ciudad: Lleida
- Ubicación: (a la derecha, según se mira, de la Vía Láctea)
- Contactar:
Re: Bateria alcalina recargable Cobre Hierro.
Buenas Rovellat
Las bombas peristálticas me interesan especialmente porque las hay de muy bajo consumo y porque además cortan el flujo de corriente a través del electrolito. La idea es utilizar el mismo depósito de electrolito, negativo y positivo respectivamente, para las celdas conectadas en serie. La diferencia de tensión entre celdas, en teoría, se colará por los tubos que suministran el electrolito. Cuando tenga esta parte en funcionamiento comprobaré hasta qué punto es importante esta derivación de corriente y como contrarrestarla.
Un tema que me sigue preocupando es el desgaste de los electrodos negativos de hierro. Estoy "bastante" seguro que parte de los mAh de descarga que media en las pruebas anteriores era fruto de consumir los electrodos de lana de hierro. Recordemos que la descarga estaba programada hasta los 0,5v por cerda, bastante por debajo de los 1,2v teóricos de la celda.
Para proteger los electrodos de hierro y aumentar el voltaje de trabajo estoy haciendo diversas pruebas añadiendo metales como el zinc, sodio o el magnesio al electrolito de la semicelda negativa.
La propuesta sería que en los ciclos de carga y descarga se deposite electrolíticamente y se consuma un metal con un potencial de reducción menor que el del Fe, aumentando así el voltaje y protegiendo además la base de hierro. Si funciona podría aumentar la tensión mínima de descarga por celda a 0,7 o 0,8v evitando consumir el hierro. De momento he probado con zinc, con resultados esperanzadores y ahora estoy probando también con magnesio,
Como apunte... por si alguien se le ocurre hacer lo mismo. El zinc (metálico) se disuelve lentamente en el electrolito de FeCl2 y restos de HCl liberando hidrógeno. Pero el magnesio se disuelve en una reacción exotérmica bastante más agresiva liberando abundante espuma (hidrógeno). Se corre el peligro de desbordar el recipiente que contiene el electrolito con la espuma o fundirlo por el calor si este es de plástico.
En mi caso he disuelto directamente el metal en el electrolito para no incrementar la proporción de iones Cl-. Una prueba interesante seria disolver cloruro de magnesio o cloruro de zinc en su caso.
De momento siguen los ciclos de carga y descarga de las celdas a razón de 400mA en la carga y 300mA en la descarga. Cada ciclo tarda unos dos días en completarse (11.000mAh) y programo 5 ciclos seguidos para tener datos comparables, así que no tendré datos concluyentes hasta final de la semana.
Las bombas peristálticas me interesan especialmente porque las hay de muy bajo consumo y porque además cortan el flujo de corriente a través del electrolito. La idea es utilizar el mismo depósito de electrolito, negativo y positivo respectivamente, para las celdas conectadas en serie. La diferencia de tensión entre celdas, en teoría, se colará por los tubos que suministran el electrolito. Cuando tenga esta parte en funcionamiento comprobaré hasta qué punto es importante esta derivación de corriente y como contrarrestarla.
Un tema que me sigue preocupando es el desgaste de los electrodos negativos de hierro. Estoy "bastante" seguro que parte de los mAh de descarga que media en las pruebas anteriores era fruto de consumir los electrodos de lana de hierro. Recordemos que la descarga estaba programada hasta los 0,5v por cerda, bastante por debajo de los 1,2v teóricos de la celda.
Para proteger los electrodos de hierro y aumentar el voltaje de trabajo estoy haciendo diversas pruebas añadiendo metales como el zinc, sodio o el magnesio al electrolito de la semicelda negativa.
La propuesta sería que en los ciclos de carga y descarga se deposite electrolíticamente y se consuma un metal con un potencial de reducción menor que el del Fe, aumentando así el voltaje y protegiendo además la base de hierro. Si funciona podría aumentar la tensión mínima de descarga por celda a 0,7 o 0,8v evitando consumir el hierro. De momento he probado con zinc, con resultados esperanzadores y ahora estoy probando también con magnesio,
Como apunte... por si alguien se le ocurre hacer lo mismo. El zinc (metálico) se disuelve lentamente en el electrolito de FeCl2 y restos de HCl liberando hidrógeno. Pero el magnesio se disuelve en una reacción exotérmica bastante más agresiva liberando abundante espuma (hidrógeno). Se corre el peligro de desbordar el recipiente que contiene el electrolito con la espuma o fundirlo por el calor si este es de plástico.
En mi caso he disuelto directamente el metal en el electrolito para no incrementar la proporción de iones Cl-. Una prueba interesante seria disolver cloruro de magnesio o cloruro de zinc en su caso.
De momento siguen los ciclos de carga y descarga de las celdas a razón de 400mA en la carga y 300mA en la descarga. Cada ciclo tarda unos dos días en completarse (11.000mAh) y programo 5 ciclos seguidos para tener datos comparables, así que no tendré datos concluyentes hasta final de la semana.
"La manzana no nos echó del paraiso, sólo nos dejó ciegos para verlo"
Cecil Thousan
Cecil Thousan
- Sergi
- Mensajes: 1723
- Registrado: Vie Mar 17, 2006 10:35 am
- País: El Segrià
- Ciudad: Lleida
- Ubicación: (a la derecha, según se mira, de la Vía Láctea)
- Contactar:
Re: Bateria alcalina recargable Cobre Hierro.
Buenas... ya os puedo aportar algunos datos interesantes. Intento resumir quince días de ciclos de carga y descarga y diversas pruebas.
En todo momento he trabajado con dos celdas en paralelo, aunque con configuraciones diferentes en cada celda para ir más rápido y testar diversos electrodos y electrolitos a la vez.
Los primeros ciclos de esta nueva fase los realicé con el electrolito sintetizado a partir de HCl y trozos de hierro disuelto en el vaso negativo y FeCl3 en el positivo. Añadí cuatro cucharadas cargadas de NaCl (sal común) en cada semicelda.
- Los electrodos positivos siempre han sido fieltro de grafito de 1cm de grosor.
- Los electrodos negativos eran lana de acero embutida en maya de hierro en la celda 1 y planas de inox en la celda 2.
Los resultados hna sido los siguientes:
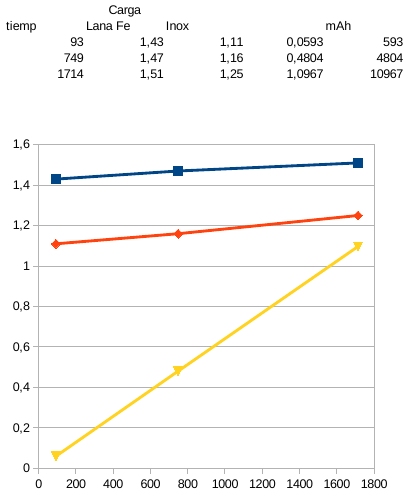
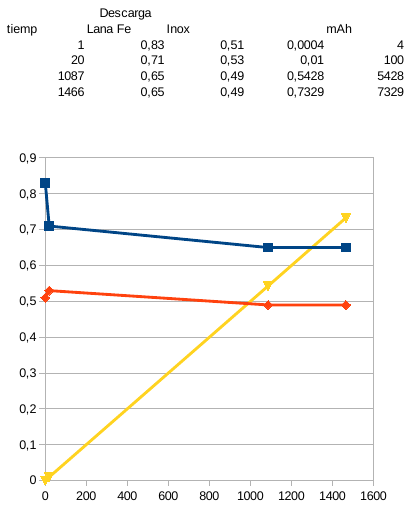
Se puede apreciar un ligero aumento de voltaje de trabajo respecto a las anteriores pruebas sin sal. En la carga un aumento de 0,5v y en la descarga de entre 0,2v y 0,3v
Se puede apreciar claramente como el electrodo negativo de lana de Fe (linea azul) trabaja mucho mejor que el de placas de inox (linea roja)
ínia roja).
En todo momento he trabajado con dos celdas en paralelo, aunque con configuraciones diferentes en cada celda para ir más rápido y testar diversos electrodos y electrolitos a la vez.
Los primeros ciclos de esta nueva fase los realicé con el electrolito sintetizado a partir de HCl y trozos de hierro disuelto en el vaso negativo y FeCl3 en el positivo. Añadí cuatro cucharadas cargadas de NaCl (sal común) en cada semicelda.
- Los electrodos positivos siempre han sido fieltro de grafito de 1cm de grosor.
- Los electrodos negativos eran lana de acero embutida en maya de hierro en la celda 1 y planas de inox en la celda 2.
Los resultados hna sido los siguientes:


Se puede apreciar un ligero aumento de voltaje de trabajo respecto a las anteriores pruebas sin sal. En la carga un aumento de 0,5v y en la descarga de entre 0,2v y 0,3v
Se puede apreciar claramente como el electrodo negativo de lana de Fe (linea azul) trabaja mucho mejor que el de placas de inox (linea roja)
ínia roja).
"La manzana no nos echó del paraiso, sólo nos dejó ciegos para verlo"
Cecil Thousan
Cecil Thousan
- Sergi
- Mensajes: 1723
- Registrado: Vie Mar 17, 2006 10:35 am
- País: El Segrià
- Ciudad: Lleida
- Ubicación: (a la derecha, según se mira, de la Vía Láctea)
- Contactar:
Re: Bateria alcalina recargable Cobre Hierro.
En la siguiente serie de experimentos añadí Zn (metálico) a la primera celda y Mg metálico en la segunda celda. Recordar que el magnesio se disuelve en ácido clorhídrico con reacción exotérmica bastante agresiva, liberando abundante espuma (hidrógeno) y calentando el electrolito. Hay que tener cuidado. Añadí los dos componentes hasta saturar el electrolito en cada caso. Recordemos que la segunda celda aún conserva el electrodo negativo de placas de inox. El resultado es el siguiente:
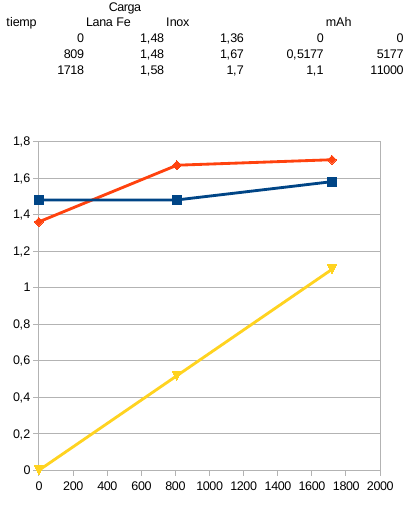
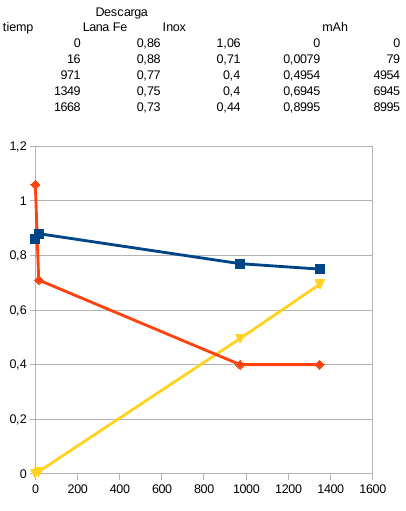
Se puede apreciar un aumento significativo de tensión de trabajo, tanto en la carga como en la descarga, en las dos celdas. Sobre todo en la celda con aditivo de Mg. Aunque con un comportamiento desigual en la descarga al tener electrodos de naturaleza muy diferentes.
Finalmente monté dos electrodos negativos iguales de lana de acero embutida en maya de hierro. Mantuve el aditivo de zinc y magnesio respectivamente en cada celda y los sometí a cinco ciclos de cargas y descargas. 400mA en la carga y 300mA en la descarga. todos los ciclos con limites de trabajo de 11.000mAh. Recuerdo que trabajo con 500 cm3 de elecrolito en cada vaso de semi-celda. (las lecturas en mAh no llegan en su mayoría al límite de 11.000mAh porque les muestras las he recogido a mano y no siempre estaba en el laboratorio justo cuando acababa el ciclo)
El resultado es el siguiente:
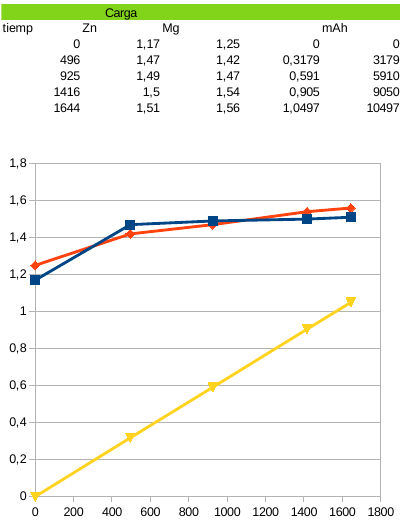
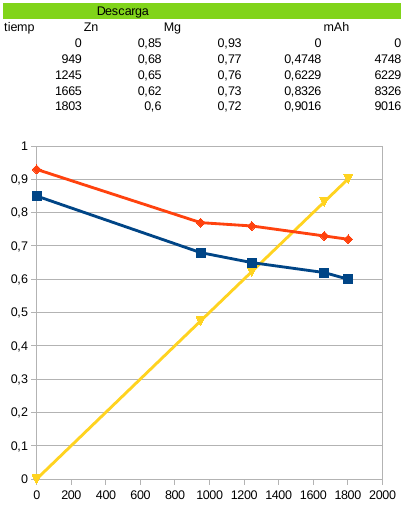
Se aprecia un ligero aumento de voltaje de trabajo en la carga en la celda con Magnesio (línea roja) respecto a la celda con zinc (línea azul)
En la descarga la diferencia de voltaje de trabajo es más acusada superando en 0,11v la celda con aditivo de magnesio.
Los datos indican una mejora sustantiva en el voltaje de trabajo y en la capacidad. Todas la descarga aportaron los 11.000mAh de la carga. Aunque parte de la capacidad se debía al desgaste de los electrodos como se verá más tarde. Sin aditivos, las celdas trabajaban sobre los 0,5v en el punto más bajo de descarga. Ahora trabajan sobre los 0,6 y 0,72v respectivamente.
Otro dato muy significativo de estas pruebas ha sido el desgaste desigual de los electrodos. Recordemos que un problema importante con el que me topé en las anteriores pruebas sin aditivos era el desgaste acelerado de los electrodos negativos de lana de acero.
En estas nuevas pruebas se puede apreciar un desgaste también importante en el electrodo de la celda con zinc. Se ha disuelto parcialmente hasta la maya de hierro. Se pueden apreciar deposiciones de zinc electrolítico (machas gris azulado). Si bien es cierto que la velocidad a la que se consume el electrodo es menos que sin zinc, no es sostenible en una batería de uso continuado.

En cambio, en la celda con aditivo de magnesio, en la semi-celda negativa, el desgaste del electrodo ha sido casi nulo. También se aprecian deposiciones de magnesio electrolítico. La estructura de la lana de acero se ha modificado sustancialmente, convirtiéndose en una especie de masa quebradiza. Pero aparentemente no ha perdido material, a diferencia del primer electrodo (zinc) en el que si ha desaparecido una parte importante del material.

De momento continuaré trabajando con Magnesio en la semi-celda negativa. Ya os contaré nuevos avances.


Se puede apreciar un aumento significativo de tensión de trabajo, tanto en la carga como en la descarga, en las dos celdas. Sobre todo en la celda con aditivo de Mg. Aunque con un comportamiento desigual en la descarga al tener electrodos de naturaleza muy diferentes.
Finalmente monté dos electrodos negativos iguales de lana de acero embutida en maya de hierro. Mantuve el aditivo de zinc y magnesio respectivamente en cada celda y los sometí a cinco ciclos de cargas y descargas. 400mA en la carga y 300mA en la descarga. todos los ciclos con limites de trabajo de 11.000mAh. Recuerdo que trabajo con 500 cm3 de elecrolito en cada vaso de semi-celda. (las lecturas en mAh no llegan en su mayoría al límite de 11.000mAh porque les muestras las he recogido a mano y no siempre estaba en el laboratorio justo cuando acababa el ciclo)
El resultado es el siguiente:


Se aprecia un ligero aumento de voltaje de trabajo en la carga en la celda con Magnesio (línea roja) respecto a la celda con zinc (línea azul)
En la descarga la diferencia de voltaje de trabajo es más acusada superando en 0,11v la celda con aditivo de magnesio.
Los datos indican una mejora sustantiva en el voltaje de trabajo y en la capacidad. Todas la descarga aportaron los 11.000mAh de la carga. Aunque parte de la capacidad se debía al desgaste de los electrodos como se verá más tarde. Sin aditivos, las celdas trabajaban sobre los 0,5v en el punto más bajo de descarga. Ahora trabajan sobre los 0,6 y 0,72v respectivamente.
Otro dato muy significativo de estas pruebas ha sido el desgaste desigual de los electrodos. Recordemos que un problema importante con el que me topé en las anteriores pruebas sin aditivos era el desgaste acelerado de los electrodos negativos de lana de acero.
En estas nuevas pruebas se puede apreciar un desgaste también importante en el electrodo de la celda con zinc. Se ha disuelto parcialmente hasta la maya de hierro. Se pueden apreciar deposiciones de zinc electrolítico (machas gris azulado). Si bien es cierto que la velocidad a la que se consume el electrodo es menos que sin zinc, no es sostenible en una batería de uso continuado.

En cambio, en la celda con aditivo de magnesio, en la semi-celda negativa, el desgaste del electrodo ha sido casi nulo. También se aprecian deposiciones de magnesio electrolítico. La estructura de la lana de acero se ha modificado sustancialmente, convirtiéndose en una especie de masa quebradiza. Pero aparentemente no ha perdido material, a diferencia del primer electrodo (zinc) en el que si ha desaparecido una parte importante del material.

De momento continuaré trabajando con Magnesio en la semi-celda negativa. Ya os contaré nuevos avances.
"La manzana no nos echó del paraiso, sólo nos dejó ciegos para verlo"
Cecil Thousan
Cecil Thousan
- Sergi
- Mensajes: 1723
- Registrado: Vie Mar 17, 2006 10:35 am
- País: El Segrià
- Ciudad: Lleida
- Ubicación: (a la derecha, según se mira, de la Vía Láctea)
- Contactar:
Re: Bateria alcalina recargable Cobre Hierro.
Después de un parón obligado de varios meses, retomo los trabajos con la batería de flujo.
He estado trabajando en los componentes del segundo prototipo de batería. Esta vez si será una verdadera batería de flujo. Las anteriores pruebas las realicé con el electrolito contenido en el mismo recipiente donde albergaba los electrodos, sin circulación.
Para poder controlar con detalle la circulación de los electrolitos en las celdas de la batería he construido un sencillo controlador de motores DC que permite ajustar el funcionamiento de las bombas peristálticas.



Básicamente, es un circuito generador de diente de sierra a base de un inversor trigger schmitt (40106 en mi caso) y dos generadores de amplitud de pulso con operacional (TL082). Como fuente de alimentación, la siempre sufrida fuente ATX vieja de ordenador. El voltímetro lo conectaré a las celdas para monitorizarlas fácilmente.
Las bombas peristálticas funcionan a 3v por lo que la tensión de 3,3v de la fuente ATX va de perlas en este caso.
De momento he montado dos bombas, pero el módulo tiene capacidad para 6 si fuese necesario ampliar.


El controlador de flujo permite ajustar ciclos de trabajo desde 2 segundos hasta 0,2 segundos y amplitud de pulso en cada bomba desde 0 hasta el 100% en cada ciclo. Esto permite ajustar el rango de trabajo de cada bomba. No funciona en régimen de PWM porque que al bajar el voltaje del motor la bomba no tiene suficiente fuerza para impulsar el líquido. Ajusta el tiempo que está funcionando respecto al tiempo que está parada la bomba peristáltica, trabajando por pulsos.
Aún tengo que comprobar el caudal mínimo ajustable, pero a razón de dos vueltas de bomba por minuto imagino que será de muy pocos ml/min. El caudal máximo de las bombas a régimen 100% de funcionamiento es de 90 ml/min. También permite invertir el sentido de circulación de las bombas para poder vaciar de electrolito fácilmente les celdas de la batería antes de desmontarlas para comprobaciones.
He estado trabajando en los componentes del segundo prototipo de batería. Esta vez si será una verdadera batería de flujo. Las anteriores pruebas las realicé con el electrolito contenido en el mismo recipiente donde albergaba los electrodos, sin circulación.
Para poder controlar con detalle la circulación de los electrolitos en las celdas de la batería he construido un sencillo controlador de motores DC que permite ajustar el funcionamiento de las bombas peristálticas.



Básicamente, es un circuito generador de diente de sierra a base de un inversor trigger schmitt (40106 en mi caso) y dos generadores de amplitud de pulso con operacional (TL082). Como fuente de alimentación, la siempre sufrida fuente ATX vieja de ordenador. El voltímetro lo conectaré a las celdas para monitorizarlas fácilmente.
Las bombas peristálticas funcionan a 3v por lo que la tensión de 3,3v de la fuente ATX va de perlas en este caso.
De momento he montado dos bombas, pero el módulo tiene capacidad para 6 si fuese necesario ampliar.


El controlador de flujo permite ajustar ciclos de trabajo desde 2 segundos hasta 0,2 segundos y amplitud de pulso en cada bomba desde 0 hasta el 100% en cada ciclo. Esto permite ajustar el rango de trabajo de cada bomba. No funciona en régimen de PWM porque que al bajar el voltaje del motor la bomba no tiene suficiente fuerza para impulsar el líquido. Ajusta el tiempo que está funcionando respecto al tiempo que está parada la bomba peristáltica, trabajando por pulsos.
Aún tengo que comprobar el caudal mínimo ajustable, pero a razón de dos vueltas de bomba por minuto imagino que será de muy pocos ml/min. El caudal máximo de las bombas a régimen 100% de funcionamiento es de 90 ml/min. También permite invertir el sentido de circulación de las bombas para poder vaciar de electrolito fácilmente les celdas de la batería antes de desmontarlas para comprobaciones.
"La manzana no nos echó del paraiso, sólo nos dejó ciegos para verlo"
Cecil Thousan
Cecil Thousan
- Diego Gonzalez
- Mensajes: 2414
- Registrado: Lun Dic 17, 2007 10:59 pm
- Ubicación: Oviedo Asturias
- Contactar:
Re: Bateria alcalina recargable Cobre Hierro.
Hola Sergi.
Ya echaba de menos las actualizaciones...
Ya tienes esas bombas y no hay nada que hacer más que echarlas a andar, pero sé que sabes que las hay peristalticas con motores pap y las veo mas adecuadas. Sin embargo me agrada ver mucho la solución que estas tratando de buscar con la electrónica que llevas montada.
Saludos
Ya echaba de menos las actualizaciones...
Ya tienes esas bombas y no hay nada que hacer más que echarlas a andar, pero sé que sabes que las hay peristalticas con motores pap y las veo mas adecuadas. Sin embargo me agrada ver mucho la solución que estas tratando de buscar con la electrónica que llevas montada.
Saludos
Mi humilde rincon web
http://sites.google.com/site/skygaps/
http://sites.google.com/site/skygaps/
¿Quién está conectado?
Usuarios navegando por este Foro: Google [Bot] y 0 invitados